事業進捗報告会 書き起こし記事
実施日時:2023年9月29日(金)
登壇者
代表取締役社長 浦田 泰生
ファシリテーター 櫻井 英明
(ストックウェザー株式会社「兜町カタリスト」編集長)
免責事項について
オンコリスバイオファーマ(以下、「当社」)は、以下に記載の情報についてあらゆる面から細心の注意を払っています。 しかしながら、当社は下記に掲載される情報の最新性・有用性・網羅性その他内容についてのいかなる保証も行うものではありません。また、当社は事前にお知らせすることなく、当社の判断によって公開されている情報の追加、変更、修正、削除、公開中断、公開中止等を行う場合があります。当社は、ご利用者各位が情報の掲載、追加、変更、修正、削除、公開の中断、中止等により生じたいかなる損害についても責任を負うものではありません。下記情報の掲載は、投資勧誘を目的としたものではありません。実際に投資を行う際は、ご利用者各位のご判断で行うようにお願い致します。さらに、下記記載の情報のうち、将来的な事項については、事情の変化等により変更されることがありうることをご留意ください。以上の点について、あらかじめご了承ください。

- 代表取締役社長浦田泰生(以下、浦田):
- 今回の事業進捗報告会では、「2023年にオンコリスに期待頂きたいこと」のうち、主に赤いチェックマークがついている箇所について、説明差し上げたいと思います。

- 浦田:
- 当社は、9月25日開示のプレスリリース において、当社とコーネル大学、免疫チェックポイント阻害剤(以下、CPi)を販売している大手製薬企業の三者間での共同開発体制が基本合意に達したことを発表いたしました。
ASCO2023で発表したとおり、コーネル大学では、テロメライシンとCPiの併用により、病勢が進んだStage4胃がん患者さま16例のうち3例で長期生存が確認されました。
余命半年ほどの患者さまが多い中で3年間生きることができた患者さまがおり、また1名の患者さまは脳転移も含めて完全にがんが消失したと認められています。これは非常に良い結果であるとご評価頂きましたが、今後どのように開発していくべきかコーネル大学と協議を続けてきました。スライド左側をご覧ください。以前は1次治療としてCPiだけの治療が行われていましたが、現在のアメリカではガイドラインで化学療法も併用しなければならないことになっています。そのような状況で、我々もCPi+化学療法にテロメライシンを上乗せして臨床試験をやらなければなりません。これは非常に大変なことであり、コーネル大学の先生方に伺ったところ、「アメリカで困っているのは2次治療である」ということが分かりました。1次治療では大体7割の患者さまで治療が失敗すると考えられています。テロメライシンはCPiが効かなくなった患者さまの反応性を再び高めるという結果が認められているため、1次治療で失敗した患者さまに、CPiとテロメライシンを併用すれば、より良い結果が得られるではないかと考えました。他の製薬メーカーも参入しておらず空白な治療の隙間を敢えて狙うことにより、ニッチな領域で許可取得ができる可能性が見えたため、臨床試験を進めていくことになりました。開発体制については、これまで通り当社とコーネル大学で臨床試験を続けていく方法もありましたが、CPiを販売している大手製薬会社と協議してCPiサンプルや資金を出して頂き、臨床試験を支えていく体制について合意が得られました。あとは契約書にサインするだけの状況に来ております。
- 櫻井英明氏(以下、櫻井):
- このトライアングルは良い形ですね。
- 浦田:
- 当初は、相手企業様に声を聞いて貰えず、このトライアングルの構築は非常に困難であると感じていました。しかし、空白の治療領域である二次治療のプロトコルを提出したところ、俄然やる気になってくれたというところが大きかったと思っています。
- 櫻井:
- 余命幾ばくも無い重症の患者さまが3年以上生存した、というのは凄いことではないですか。
- 浦田:
- 16例中3例という少ない症例ですが、それ程効果のある患者さんがいたということは重要な発見だったと思っています。特に、「脳転移をしている患者さんで転移部位も消えたというのは、画期的な結果である」というのがコーネル大学の考えです。また、化学療法は苦しい治療を続けながら何とかご存命になっていく中で、テロメライシンには重い副作用がないというところが一つの訴求ポイントになってくると考えています。
- 櫻井:
- 今回の開発体制の一番のポイントはどこでしょうか。
- 浦田:
- 一番のポイントは、臨床試験にかかる資金・リソースを両社で分担した契約になる見込みであることです。医師主導治験に対して、当社はテロメライシンを無償で提供し、相手企業さまもCPiの治験サンプルを無償で提供して頂きます。それに加えて試験経費もかかりますが、これも両社で負担していきます。コーネル大学の考えた新しい適応に向けた臨床試験を、当社と相手企業さまで支えていくことは、非常に意味のある体制であると考えています。
- 櫻井:
- 「相手企業による開発費の負担は、テロメライシンへの期待の表れ」と見ても宜しいのでしょうか。「コストも応分に出しますよ」ということですから一歩先を見据えながら、と理解できますよね。
- 浦田:
- はい。私はそう信じております。相手企業さまもそう考えていますが、1次治療を失敗した患者さまは、2次治療は苦しい化学療法しかなく、そのうえ手術もがんが転移しているため困難です。我々は、1次治療を失敗した7割の患者さまに対して1つの希望を与えられることは、メーカーにとって非常に重要なことだと考えています。
- 櫻井:
- 相手先の企業名はいつ頃公表されますか。また、臨床試験はいつ頃開始されますか。
- 浦田:
- コーネル大学の先生方は、臨床試験を来年早々にはスタートさせたいと考えています。相手企業さまも契約内容について合意しているため、我々にもコーネルから契約書が届いたと考えていますが、コーネル大学も相手企業さまも大きな組織ですので、最後のサインに少し時間がかかるかもしれません。しかし、少なくとも、来年早々に臨床試験をスタートできるように三者が契約を急いでいる状況です。
- 櫻井:
- 契約ですから、齟齬があってもいけませんし、十分なチェックをしながら進めていくということですね
- 浦田:
- もちろん、契約書にサインがされれば、相手企業さまの名前の公表はできるのではないかと考えており、あと少しだと思います。
- 浦田:
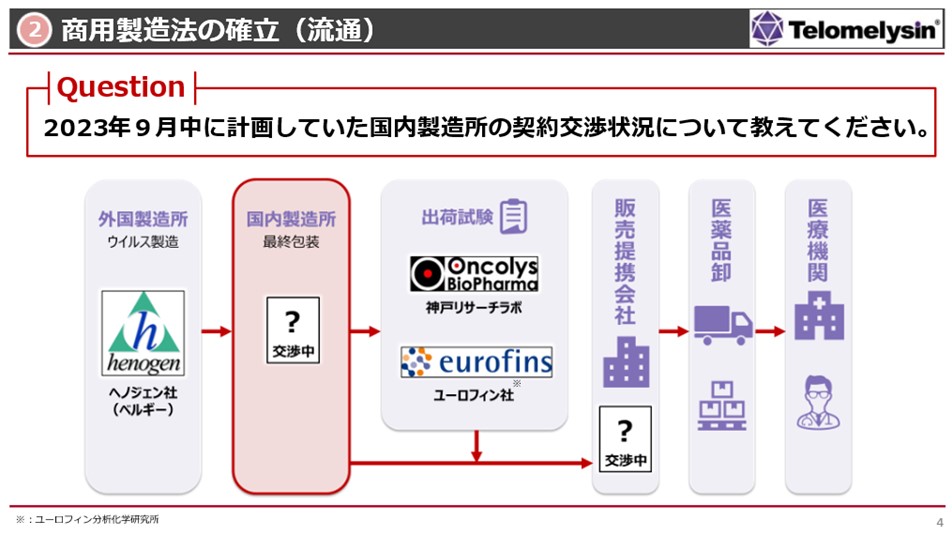
- 次に、商用製造に関連する「国内製造所の契約交渉状況」について説明いたします。ベルギーのヘノジェン社で、ウイルスの原液を作って瓶詰めを行い、日本国内に持ってきます。国内製造所では箱詰めをして最終包装を行った上で保管し、当社神戸リサーチラボと京都にございますユーロフィン社で出荷試験を行い、販売提携先や卸を通じて各病院に届きます。
国内製造所に関しては、今年初めからご縁がありました1つの製造所と「何とかビジネスを進めましょう」と話を進めてきました。しかし、本夏より候補先企業様から新たに幾つか条件を提示され、我々もその条件に対応しなければならなくなりました。当初は9月末に決めようと思っていた国内製造所との契約は、結果として遅れることになりました。ただし、将来の承認申請・実際の販売には影響がない範囲内での遅れにするようにいたします。かなり早めに話し合いを行っていたため、早くに契約をできると考えていましたが、来年できるだけ早い時期までに、今後6か月以内に契約を締結したいと考えています。 - 櫻井:
- 一方で、販売提携会社との交渉進捗はどのような状況でしょうか。
- 浦田:
- 販売会社については、多くの国内製薬メーカー様とお話ししております。食道がんというニッチな領域に対応ができるかどうか、販売費の料率など、相手企業様に応じて様々なパターンを検討していく必要があり、引き続き提携交渉については動いている状況です。後ほどご説明させて頂きますが、10月に当社からテロメライシンのトップラインデータを報告することになっております。幾つかの企業様からは、「一旦Declineしたけれども、その結果を見てもう一度考え直したい」と、またお声を掛け頂いた先もあります。国内販売パートナーは年内には決めようと思っており、これまでの皆さまへのお約束通りに動いているという状況でございます。
- 櫻井:
- 3つの方程式を解いているということですね。「製造」と「販売」と「トップラインデータの結果」、この3つの最適解を見つけようとしている。進捗はしていますが、あとはテクニカルな問題ですね。お話頂いた料率をどうするとか、ここはもう交渉次第ですね。
- 浦田:
- 相当タフな交渉です。
- 浦田:
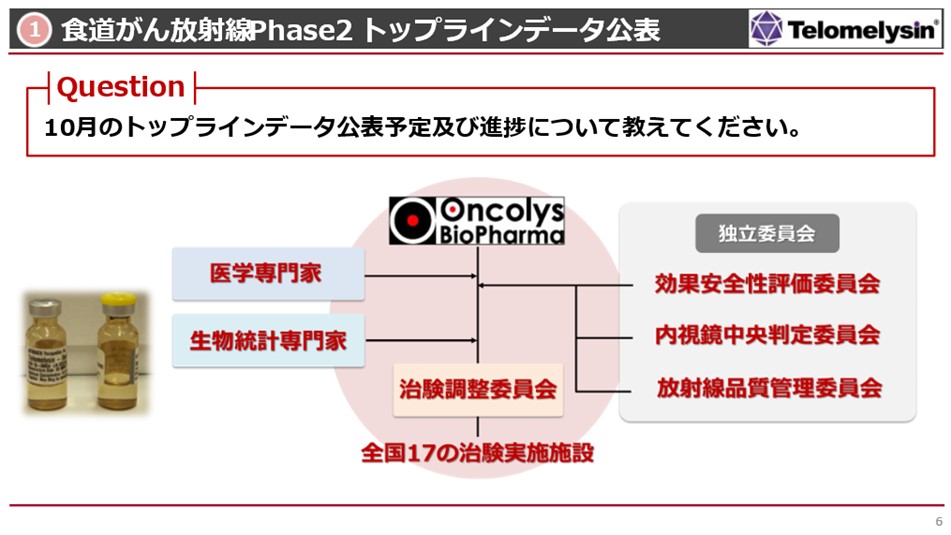
- トップラインデータの公表予定について、説明いたします。当社が一番期待しているところで、私も19年オンコリスでやってきて、「この結果を出すために会社をやってきた」というようなものです。臨床試験のデータは、生存者の確認やフォローアップの臨床検査値など非常に多岐にわたりますが、既にデータはほぼ纏まっており、統計解析結果の大筋は出てきているようです。この結果に対して、各専門家・各委員会の先生方と色んな話し合いを積み重ねまして、「この臨床試験はちゃんとできている」という判断を頂いております。そういう意味で、「この臨床試験のトップラインデータを10月に公表させて頂くことは十分可能である」という状況にきております。
- 櫻井:
- 専門家の方々・評価委員会の先生方も、真剣にやられているわけですね。
- 浦田:
- 私が想像したよりもずっと真剣に取り組んで頂いております。食道がんというのは薬がないわけですから、先生方も「自分たちの診療でこの薬が本当に使えるのかどうか」という目線で見ておられ、真剣に評価して頂いております。
- 櫻井:
- そういう意味ではもちろん厳しい審査を受けているということですけれども、今年度のビッグイベントになるということですよね。
- 浦田:
- オンコリス始まって以来のビッグイベントです。
- 櫻井:
- 「データの開示は10月から変更ない」ということで宜しいですね。
- 浦田:
- ないです。不変です。

- 櫻井:
- 最後に投資家さんから頂いた事前質問です。12月12日~14日に開催される第8回オンコリティック・バイオセラピー・サミットにオンコリスUSAが参加するようですが、その詳細情報を教えてください。
- 浦田:
- これは、オンコリスUSA社長のTaliaが、腫瘍溶解性ウイルス及びがん治療の領域に幅広い人脈を持っておりますので、このサミットでシンポジストを務めることになりました。彼女が、テロメライシンの国内トップラインデータについて発表するかどうかは未定ですけれども、少なくともテロメライシンのこれまでの臨床試験の結果などを話す予定です。世界の数十社の腫瘍溶解性ウイルス治療薬開発を行っている企業と情報交換をするサミットに、シンポジストとして参加するというわけでございます。
- 櫻井:
- 参加されるのはオンコリスのアメリカ子会社ですから、同業他社含む世界中の腫瘍溶解性ウイルスに関わるステークホルダーからオンコリスに対する注目・意識を集めるという理解で宜しいでしょうか。
- 浦田:
- そうですね。アジアで頑張っているバイオベンチャーであることと、食道がんという珍しい病気で頑張っている企業として注目を受けて、Taliaが呼ばれたということになります。
- 櫻井:
- 私は以前から、もし食道がんや胃がんになるとしたら、テロメライシンができてからが良いと申し上げていますが、この半年、1年くらいでかなり状況が変わってきていますね。
- 浦田:
- データが集まってきていることと、ヘノジェンでの製造などは非常に大きい進捗だったと思います。
- 櫻井:
- 本日は貴重なお話を頂き有難うございました。最後に投資家の皆さまへメッセージをお願いします。
- 浦田:
- 株主の皆さまにも、大変期待をして頂いていることは身にしみて感じております。10月のトップラインデータにつきましては、良い報告ができるようにしたいと考えております。また、テロメライシンの製造も、商用製造に向けてもう1段・2段のステップを上らなければならないですが、目途が見えてきています。あとは、販売会社や国内の最終包装の役割を担う製造所と提携することで、遅滞なく承認申請を行いその後の許可を得ていくことに、全社一丸となって全力投球していきたいと思います。
以 上













